近日,病毒学国家重点实验室/武汉大学泰康医学院(基础医学院)/武汉大学泰康生命医学中心夏宇尘教授课题组在国际学术期刊PLOS Pathogens在线发表题为“Hepatitis B virus RNAs co-opt ELAVL1 for stabilization and CRM1-dependent nuclear export”的研究论文。该研究使用RNA Pulldown-液质联用质谱技术筛选出潜在的乙型肝炎病毒(hepatitis B virus,HBV)RNA出核关键调控因子ELAVL1。通过细胞和动物模型确认该分子在HBV RNA识别、稳定性维持和出核调控过程中发挥核心功能,并对详细分子机制进行了探究。

目前,全球HBV慢性感染者已高达2.96亿人,其中大约三分之一在中国。乙肝病毒感染者发生肝硬化和肝癌的几率高,我国每年约有30-40万人死于乙肝病毒导致的肝病。虽然目前有针对乙肝病毒的疫苗和药物,但慢性乙型肝炎仍很难被完全治愈。因此,迫切需要寻找新的药物靶点来清除乙肝病毒。HBV RNA出核是病毒复制中重要的转录后调控过程,它是病毒翻译合成蛋白质的关键环节,也是病毒在细胞质中通过反转录复制基因组的必要过程。然而,目前HBV RNA出核的分子机制尚不明确。
为回答这一关键科学问题,夏宇尘教授课题组通过体外转录合成HBV RNA后通过RNA Pulldown富集其潜在互作宿主因子,并使用液质联用质谱技术鉴定出60个富集因子。通路分析提示ELAVL1介导的RNA调控通路与HBV相关,而蛋白互作组学和基因聚类分析则提示ELAVL1和CRM1发挥核心作用。在HBV感染的人肝原代细胞和HepG2-NTCP细胞中敲降ELAVL1表达会导致细胞培养上清中HBV DNA、HBeAg和HBsAg的减少。ELAVL1敲降抑制了细胞内的HBc相关HBV DNA水平和HBc蛋白表达,但不影响HBV cccDNA的水平。该结果在HBV复制小鼠模型中得到印证。这些结果提示ELAVL1作为促病毒宿主因子,在cccDNA形成后阶段调控HBV复制。研究人员随后对胞内HBV RNA水平的的进一步观察发现,ELAVL1的敲除降低了细胞质和细胞核中的HBV RNA水平。RNAscope实验证实了ELAVL1的敲降对HBV RNA亚细胞水平的抑制作用,但这不影响病毒阳性细胞的比例。研究团队随后发现ELAVL1的敲降并不影响HBV启动子和增强子的活性,但加速了HBV RNA的降解。综上所述,这些结果表明ELAVL1参与了HBV RNA的转录后调控。
在此基础上,研究人员解析了ELAVL1调控病毒RNA的详细分子机制。ELAVL1是一个具有稳定RNA并参与其出核的分子。通过对不同基因型HBV序列和不同转录产物序列比对,研究人员发现除HBx RNA外,HBV RNA上存在保守的AU-rich element(ARE)元件。该元件突变会抑制HBV RNA和ELAVL1的相互作用。ELAIVL1在与HBV RNA结合后会与具有出核信号肽段的桥接分子ANP32A和ANP32B相结合,这两个蛋白进而招募CRM1,将出核信号传递给该分子,最终介导病毒RNA出核。另外,研究者对HBV RNA的降解机制进行探究发现通过结合HBV RNA,ELAVL1还保护病毒RNA免受DI3+RRP6+ RNA exosome降解的影响。团队还对ELAVL1成为药物靶点的可能性进行了评估。使用ELAVL1-ARE结合竞争性抑制剂CMLD-2处理会一定程度上抑制HBV产毒细胞中胞质和胞核中HBV RNA水平以及上清液中HBV DNA、HBeAg和HBsAg的水平。这些结果提示ELAVL1可以作为抗HBV的新靶点。
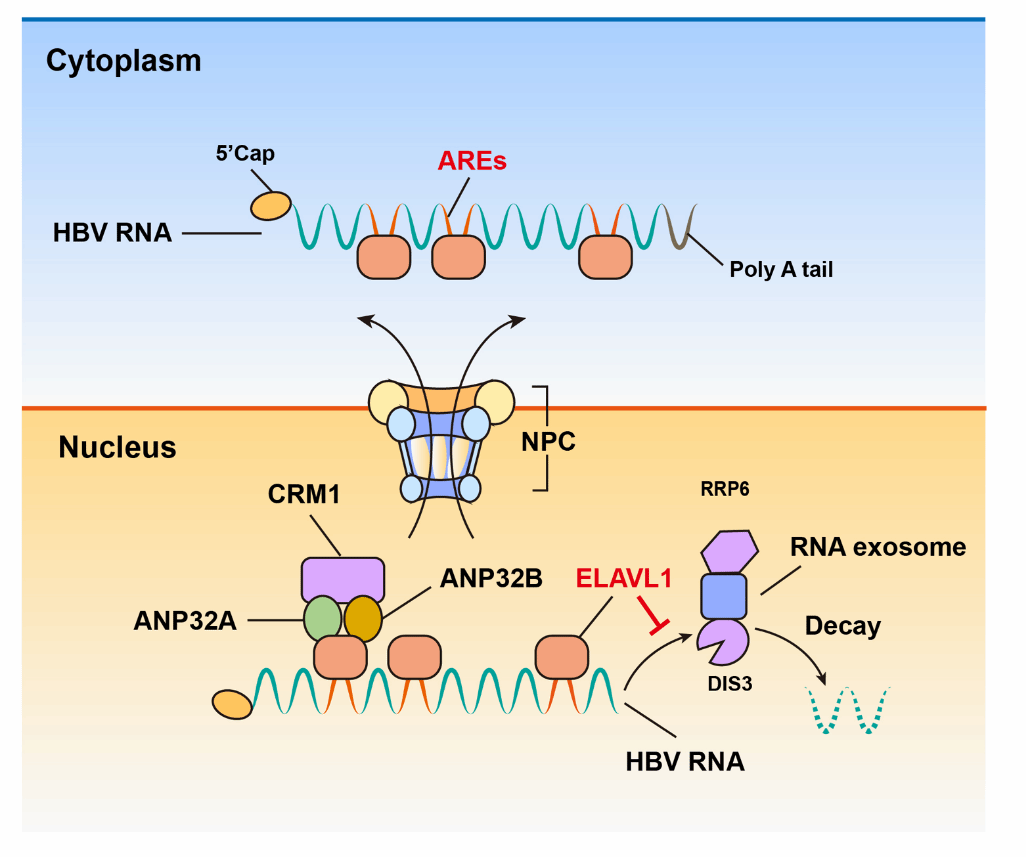
综上所述,研究者发现ELAVL1通过CRM1途径将HBV RNA从细胞核“护送”至细胞质。ELAVL1通过病毒RNA中的ARE元件与HBV RNA结合,进而与ANP32A和ANP32B相结合,将出核信号传递给CRM1,将病毒RNA从细胞核运出。通过与HBV RNA结合,ELAVL1还保护病毒RNA免受DI3+RRP6+ RNA exosome降解的影响。
该研究得到平原实验室开放课题重点项目(2023PY-OP-0101)、国家自然科学基金(81971936)、湖北省医学青年拔尖人才等项目资助。武汉大学基础医学院博士后郑颖城、博士生王梦飞为该论文共同第一作者,夏宇尘教授为通讯作者。
夏宇尘教授2018年通过海外高层次人才计划回国后一直致力于病毒性肝炎的研究,在乙肝病毒实验模型的建立、病毒宿主相互作用机制和新型抗病毒治疗手段上做了一系列的工作,作为通讯作者在Journal of Hepatology, PNAS,Hepatology, Nature Metabolism, Plos Pathogens, Cellular and Molecular Gastroenterology and Hepatology,Journal of Virology,Journal of Biological Chemistry,Emerging Microbes & Infections,Antiviral Research等学术期刊发表20余篇研究论文。实验室招收博士后1-2名,详情请联系yuchenxia@whu.edu.cn。