近日,病毒学国家重点实验室陈宇教授与熊义博士等研究团队合作在国际学术期刊Cell Death & Disease在线发表了题为“A broad neutralizing nanobody against SARS-CoV-2 engineered from an approved drug”的研究论文。该论文以商业化纳米抗体为骨架,构建了1010数量级的工程化纳米抗体文库,并利用噬菌体展示技术从该文库中筛选到多株新型冠状病毒纳米抗体,其中纳米抗体VHH60表现出高效且广谱的新冠病毒中和活性。利用该工程化的纳米抗体文库能够在短时间内筛选得到特异性纳米抗体,在应对未来有大流行风险的传染病具有积极意义。

自2019年年底COVID-19暴发以来,带来了全球卫生和经济危机。利用中和抗体阻断病毒突刺蛋白(Spike)与宿主受体的相互作用是抑制病毒感染的有效途径。在各种来源于人或小实验动物的单克隆抗体中,从驼类动物中发现的纳米抗体(VHH)是一类具有独特性质的抗体。纳米抗体只含有重链的单体抗原识别结构域,分子量仅为15kD,具有易于生产和操作、稳定性良好、渗透性强、免疫原性低等优点。纳米体已被广泛开发为针对癌症、自身免疫性疾病和肾脏疾病的治疗药物。
为了得到抗新冠病毒的纳米抗体,研究人员以商业化纳米抗体Caplacizumab为模板,对互补决定区(complementary determining regions, CDRs)进行工程改造,构建了筛选新冠病毒特异性纳米抗体突变体文库。研究人员基于天然VHH氨基酸序列特征,设计CDR1、CDR2与CDR3区域的氨基酸多样性。对于CDR3高度多样化区域的每个位置,引入18种氨基酸, Y、R、D、T、A、P、L、V、E、N、W、I、F、H、K、Q的频率为5%,S和G的频率为10%,排除终止密码子C和M。此外,在高度多样化的CDR3环中引入了不同长度的多样性,范围从6到17个残基。利用高速DNA诱变基因工程将氨基酸突变引入纳米抗体的CDR区,得到的纳米抗体突变体通过噬菌体展示技术展示于噬菌体表面,该文库的库容为1010数量级。利用S蛋白的RBD结构域进行3轮筛选。单克隆噬菌体ELISA鉴定RBD特异性阳性克隆。测序后鉴定出78个RBD特异性的VHH基因,并通过PCR从噬菌体中扩增出。在细胞系中表达纯化这一批纳米抗体,检测纳米抗体与hACE2对RBD的竞争结合活性,最终筛选得到7株靶向新冠病毒RBD的纳米抗体(图1)。
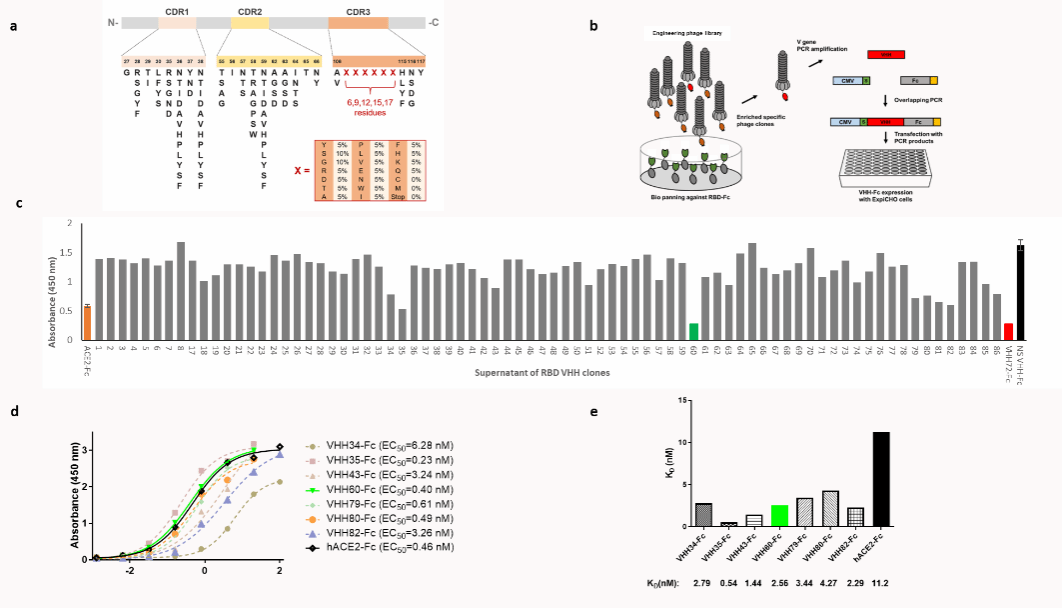
图1. 筛选RBD特异性的纳米抗体。
研究人员进一步检测了这一批纳米抗体在细胞水平和小鼠体内对新冠病毒的中和能力。实验结果显示,纳米抗体VHH60在细胞水平实验中表现出了较好的抗病毒活性(IC50=1.87±0.35 nM)。小鼠实验表明,感染前一天腹腔注射0.5 mg/kg 的VHH60,即可显著降低K18-hACE2 KI小鼠感染新冠病毒后的肺部病毒载量和病理损伤,显著提高小鼠的生存率(图2)。新冠病毒突变株不断出现,给中和抗体带来了巨大的挑战。研究人员进一步检测了VHH60对多种突变株的中和活性。实验结果表明,VHH60对几种Omicron突变株(BA.1,BA.2和BA.3)依然具有较强的中和活性,其IC50均在纳摩尔水平。
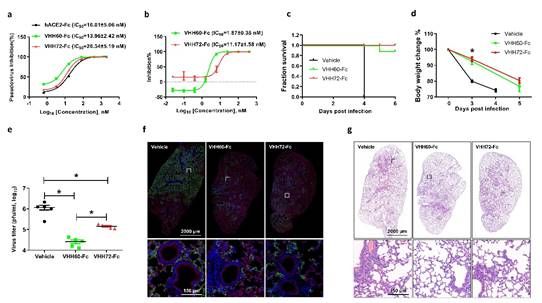
图2.纳米抗体VHH60在细胞水平和小鼠水平的抗新冠病毒效果。
最后,研究人员利用冷冻电镜技术解析了VHH60与新冠病毒Spike三聚体复合物和结构。研究结果显示,VHH60与Spike结合时,三聚体呈“1-up”构象。为了进一步揭示VHH60与RBD之间的相互作用细节,研究人员还使用蛋白质晶体学手段,获得了分辨率为3.40 Å的复合物结构。分析表明,VHH60的CDR2和CDR3与Spike的S351, S470-471和S493-494相互作用。此外,研究人员在VHH60和RBD的界面上发现了一些潜在的氢键,揭示了VHH60的CDR与RBD中的表位残基之间独特的相互作用网络。值得注意的是,VHH60的大部分结合表位与ACE2结合位点S437-508重叠,阻止了ACE2与RBD的结合(图3)。
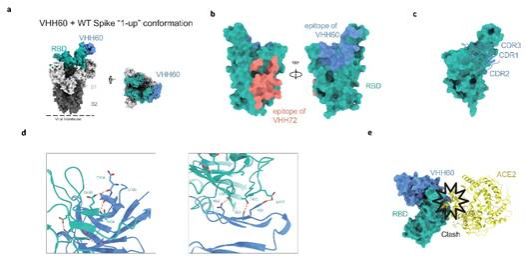
图3. VHH60与Spike复合物的结构。
总的来说,该研究建立了一种在短时间内产生针对大流行SARS-CoV-2的中和抗体的方法,包括模板合成、载体构建、文库构建、筛选、单克隆筛选、VHH-Fc表达和验证。与传统的免疫动物抗体发现方法不同,该方法节省了2至3个月的免疫时间,并且使用商业化抗体作为模板可以通过其经过验证的临床框架并降低可开发性风险。该方法在应对未来可能的大流行传染病时,具有良好的应用前景。
武汉大学病毒学国家重点实验室陈宇教授、蓝柯教授,保诺桑迪亚公司熊义博士(现深圳湾实验室)、侯信成博士(现诺诚健华)和南京大学郭航天博士为该论文共同通讯作者,武汉大学病毒学国家重点实验室刘乾运博士,上海科技大学卢宇驰,保诺桑迪亚公司蔡晨光博士(现百普赛斯)和黄燕燕(现博骥源生物)为该论文共同第一作者。该研究得到了国家重点研发计划等项目的资助,相关病毒实验在武汉大学动物实验中心/ABSL-Ⅲ实验室完成。