近日,病毒学国家重点实验室李峰研究员团队在国际学术期刊ACS Nano在线发表了一项题为“Transformation of a Viral Capsid from Nanocages to Nanotubes and Then to Hydrogels: Redirected Self-Assembly and Effects on Immunogenicity”的研究工作。该研究实现了病毒衣壳蛋白组装体从笼形到管状、再进一步到纳米管水凝胶的转变,并揭示了这种纳米形态转变带来的免疫学效应。
不同形态往往能赋予生物系统差异化的功能。生物大分子自组装是生物结构、机器乃至系统形态发生的主要途径之一,病毒是其中的典型代表。天然病毒衣壳存在两种基本形态,即正二十面体对称的球形和螺旋对称的棒状。病毒衣壳蛋白可自组装形成病毒样颗粒(virus-like particles, VLPs),广泛应用于生物医药、材料学等不同领域。当前VLP的应用与研究都是基于上述两种形态。如果能操控VLP自组装获得其它形态的结构,则可能赋予其更优异的性质或全新的功能。例如,感染人类和动物的病毒绝大多数都是球形,已获临床应用的VLP疫苗更是只有球形。如果球形VLP能转换成其它形态,对其免疫原性将产生什么影响?
围绕上述问题,李峰团队与合作者以MS2 VLP为模式体系,借助分子动力学模拟,对组装界面关键区域FG loop进行再设计,将70号位点突变为半胱氨酸,由其介导形成新的强相互作用(二硫键),打破天然正二十面体对称轴附近界面作用力的同时,引导组装单元(衣壳蛋白二聚体)形成一维结构。实验证实,上述突变联合46号位点突变(排除内源半胱氨酸潜在干扰),可使其球形纳米笼结构完全转变成超细双螺旋纳米管,平均长度约1 μm,外径8.6 nm,内径2.6 nm。高分辨冷冻电镜结构显示,突变蛋白的二级和三级结构与野生型几乎相同,但FG loop柔性有差异,组装单元形成了与野生型完全不同的排布模式。更有意思的是,70号位点突变成疏水性侧链氨基酸也能形成类似的纳米管,而突变成组氨酸则能获得单螺旋纳米管。进一步,在纳米管表面75号位点引入半胱氨酸,可引发纳米管交联形成还原响应型凝胶块体(图1)。利用该可变形组装体系,他们比较了纳米笼、纳米管和纳米管凝胶三种不同形态对MS2衣壳蛋白免疫原性的影响:相比纳米笼,纳米管可显著提升体液和细胞免疫应答水平,纳米管凝胶虽不能显著提升体液免疫应答水平,但能大大提升CD8+ T细胞的细胞因子分泌水平和细胞的杀伤功能(图2)。该工作获得了首个多层级、可变形的VLP自组装体系,揭示了组装形态对病毒衣壳蛋白免疫原性的重要影响,为纳米疫苗和其它功能蛋白纳米材料的设计提供了新思路。
中国科学院武汉病毒研究所博士研究生杨梦思、饶桂波博士和复旦大学李龙博士为该论文共同第一作者;武汉病毒研究所李峰研究员、曹晟研究员和复旦大学陈国颂教授为论文共同通讯作者;深圳理工大学张先恩研究员、上海大学魏滨教授等参与了此项研究。该研究得到了国家重点研发计划、国家自然科学基金、武汉市知识创新专项、武汉市重大科技专项等项目的支持。
文章链接:
https://pubs.acs.org/doi/10.1021/acsnano.4c01969

图1. MS2衣壳蛋白组装体由笼形到管状再到凝胶的形态操控。
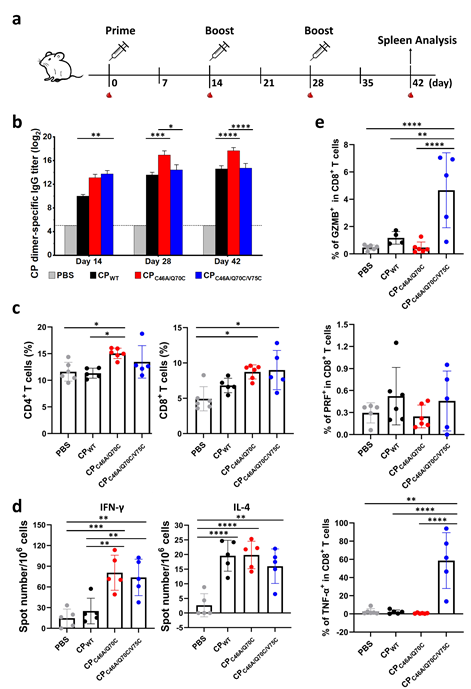
图2. 纳米组装形态显著影响MS2病毒衣壳蛋白的免疫应答。CPWT,纳米笼;CPC46A/Q70C,纳米管;CPC46A/Q70C/V75C,纳米管凝胶。