2023年4月28日,武汉大学病毒学国家重点实验室张军杰教授课题组在国际学术期刊Molecular Therapy-Oncolytics上在线发表题为“Oncolytic herpes simplex virus armed with a bacterial GBP1 degrader improves antitumor activity”的研究论文。该研究发展了一种新型溶瘤疱疹病毒改造策略,成功提高了溶瘤病毒肿瘤免疫治疗效果。
溶瘤病毒是一类野生型或经过基因改造的病毒,可以选择性在肿瘤细胞中进行复制,从而杀死肿瘤细胞,并通过激活抗肿瘤免疫反应来进一步促进治疗效果。 2015年,美国FDA批准了基于HSV-1的溶瘤疱疹病毒用于治疗黑色素瘤,并且目前还有大量的溶瘤病毒疗法在进行临床实验。尽管溶瘤病毒治疗已经取得了一定的效果,但受限于恶劣的肿瘤微环境,单独使用时疗效非常有限。因此,发展新型的溶瘤病毒,提高病毒复制水平及免疫刺激活性,是亟待解决的关键问题。
在该研究中,作者们发现HSV-1感染强烈诱导GBP蛋白家族的表达,进一步研究发现大部分GBP蛋白都能抑制HSV-1复制,其中GBP1的抑制效果最为显著。机制研究发现,GBP1通过干扰细胞骨架结构限制了HSV-1感染后病毒基因组转运进入细胞核,且GBP1的GTP酶活性及异戊烯化修饰对其抑制HSV-1复制都非常关键。此前的研究表明志贺氏菌编码的效应蛋白IpaH9.8能够有效降解包括GBP1在内的多个GBP蛋白家族成员。作者们在溶瘤疱疹病毒中重组表达了IpaH9.8(oHSV-IpaH9.8),发现在体外细胞感染中oHSV-IpaH9.8能够有效降解GBP1,显著提高病毒复制能力。在小鼠实验中,相比于原始溶瘤病毒oHSV,oHSV-IpaH9.8能更有效地抑制肿瘤生长,增强肿瘤免疫反应,表明通过靶向限制因子促进溶瘤病毒复制是一种有效的提高溶瘤免疫治疗效果的策略。
武汉大学医学研究院/免疫与代谢前沿科学中心/病毒学国家重点实验室张军杰教授为该论文的通讯作者,医学研究院2020级博士研究生谢军为该论文的第一作者,武汉大学口腔医学院孙志军教授为共同通讯作者,其他合作者还包括武汉大学蓝柯教授、伍兵教授,浙江大学潘冬立教授和汕头大学覃青松教授。该研究获得国家重点研发计划、国家自然科学基金、武汉大学双一流建设经费及病毒学国家重点实验室自主科研项目等资助。
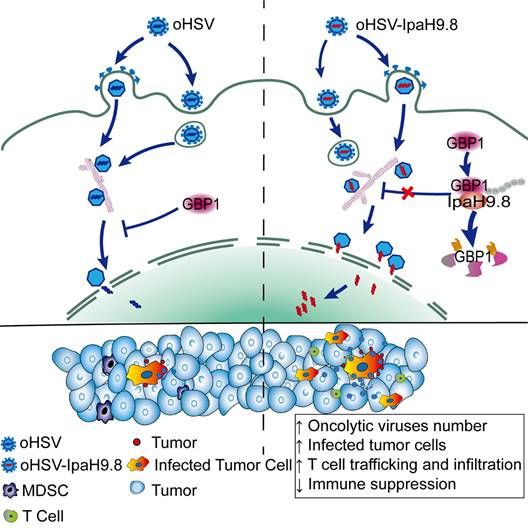
示意图:表达IpaH9.8的溶瘤疱疹病毒可以有效降解限制因子GBP1,促进病毒复制,提高溶瘤免疫治疗效果
论文链接:https://www.sciencedirect.com/science/article/pii/S2372770523000311