2022年5月12日,武汉大学病毒学国家重点实验室周海兵教授、蓝柯教授、吴叔文副教授合作在国际学术期刊Cell Insight发表题为“Discovery of Oseltamivir-Based Novel PROTACs as Degraders Targeting Neuraminidase to Combat H1N1 Influenza Virus”的研究工作,该研究利用目前药物研发热点技术—蛋白水解靶向嵌合体(PROteolysis TArgeting Chimera,PROTAC),首次报道了基于奥司他韦骨架设计的神经氨酸酶降解剂在抗流感病毒药物研发中的应用,研究显示部分PROTAC化合物能显著降解靶蛋白神经氨酸酶和抑制病毒复制,且对奥司他韦耐药株(H1N1,H274Y)也具有较好的抑制效果(EC50 = 1.31 mM),为抗流感药物的研发提供了新思路与新方法。

每年的流感暴发对人类生命健康安全造成了严重威胁。目前的抗流感药物如金刚烷胺,奥司他韦由于毒副作用或易产生耐药等局限难以完全满足患者的临床治疗需求。蛋白水解靶向嵌合体(PROteolysis TArgeting Chimera,PROTAC)是近年来蓬勃发展的一项通过体内泛素-蛋白酶体途径降解目标蛋白的新兴技术。PROTAC分子是由一定种类或长度的连接链(linker)将靶向目标蛋白和招募E3连接酶的配体分子结合在一起形成的双功能分子,在进入细胞后,首先与靶标蛋白结合并招募E3连接酶对其进行泛素化标记,随后通过体内的26S蛋白酶体降解靶标蛋白,释放出的PROTAC分子又可以进入下一个催化降解循环。目前,该技术已被广泛应用于与各种肿瘤疾病相关的药物研发领域,且由于其优越的亚催化性质、能克服药物耐药性及靶向“不可成药靶点”等优点受到广大药物化学家以及生物化学工作者的关注。
研究团队基于现有药物奥司他韦结构骨架设计、合成了一系列具有不同连接链和E3配体小分子的PROTAC化合物,其中化合物8e(连接链为烷基链,E3配体为CH3-VHL)对H1N1的抑制活性为0.33 mM,且能以剂量依赖方式降解靶蛋白神经氨酸酶NA(图1 A, B),在浓度为5.0 mM时,降解效果约为50%。为了验证化合物8e的抗病毒活性是通过其降解活性产生的,该团队设计了阴性对照化合物8e-neg,化合物羟脯氨酸部位的羟基发生了构型翻转(紫色基团),因而无法招募E3连接酶和降解靶蛋白。如图1C所示,8e-neg在单独给药时无法降解靶蛋白和抑制病毒复制,证明了化合物8e的抗病毒活性确实是通过降解NA产生的。此外,通过添加配体竞争性抑制剂如奥司他韦(OSP),E3配体(CH3-VHL)或蛋白酶体抑制剂(MG132),化合物8e的NA降解活性被显著抑制。以上结果证明8e通过泛素-蛋白酶体途径以剂量依赖方式降解NA。
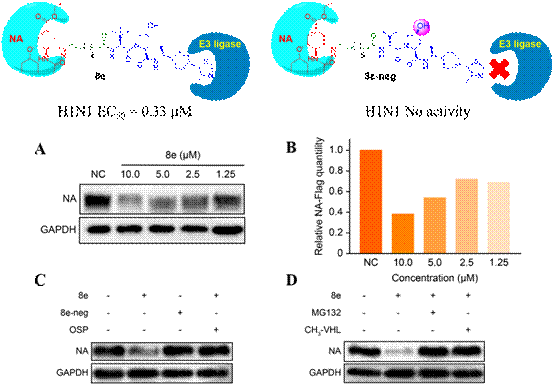
图1 奥司他韦PROTAC化合物的生物活性验证及机制探究
奥司他韦耐药性日益严重,而PROTAC技术由于能克服药物耐药性等优点备受关注。研究团队后续评估了化合物8e对奥司他韦耐药株(H1N1,H274Y)的抑制效果。如图2所示,8e能以低微摩尔水平减少病毒核蛋白NP含量及其mRNA水平,而奥司他韦未表现出明显的病毒抑制活性。这一结果说明了PROTAC技术有望缓解抗病毒药物的耐药性问题。

图2 化合物8e对奥司他韦耐药株(H1N1,H274Y)的抗病毒效果
综上,该研究工作首次报道了PROTAC技术在抗流感病毒药物研发领域中的应用,基于奥司他韦骨架设计的神经氨酸酶降解剂具有良好的抗病毒效果及靶蛋白降解能力,为抗流感药物的研发提供了新思路与新方法。
武汉大学病毒学国家重点实验室周海兵教授、蓝柯教授和吴叔文副教授为该文共同通讯作者;博士研究生许智超、刘欣瑾和麻笑雨为论文共同第一作者。该研究得到国家基金委基础科学中心(32188101)等项目的支持,项目相关技术已获得国家发明专利授权。
论文链接:https://authors.elsevier.com/sd/article/S2772-8927(22)00027-X