新冠病毒(SARS-CoV-2)引发的COVID-19疫情仍在世界各国肆虐,截止2022年2月,全球新冠肺炎累计确诊病例数超3.9亿例,累计死亡超574万例。阐析冠状病毒的免疫和病理过程对于合理设计疫苗及研发抗病毒药物至关重要。
近日,国际学术期刊mBio在线发表了我室陈宇团队与中山大学郭德银教授、瑞士伯尔尼大学Volker Thiel教授和美国爱荷华大学Stanley Perlman教授合作的最新研究论文,题为“N7-Methylation of the Coronavirus RNA Cap Is Required for Maximal Virulence by Preventing Innate Immune Recognition”(冠状病毒RNA N7-甲基化通过逃逸天然免疫所识从而实现其高病毒毒力)。该研究揭示由冠状病毒非结构蛋白14 (nsp14) 介导的RNA N7-甲基化可以辅助冠状病毒逃逸I型干扰素(IFN)介导的免疫反应。
研究人员结合前期对冠状病毒nsp14 N7-甲基转移酶功能的研究,选取了nsp14 N7-甲基转移酶的保守性关键活性位点,以鼠肝炎病毒(MHV)为研究对象,利用反向遗传学系统拯救得到了N7-甲基转移酶关键活性位点突变的重组突变病毒rMHVnsp14-Y414A。研究人员发现,相比于野生型病毒,rMHVnsp14-Y414A感染原代细胞可显著上调IFN-β的表达,并引发一系列天然免疫因子的上调。通过分别检测野生型病毒rMHV的RNA、突变病毒的RNA、以及包含不同帽子结构的RNA诱导的IFN-β水平,研究人员确认rMHVnsp14-Y414A诱导的天然免疫反应上调与其RNA帽子的N7-甲基化活性相关(图1)。

图1. rMHVnsp14-Y414A感染原代细胞时IFN-β表达上调
随后研究人员分别用rMHV和rMHVnsp14-Y414A感染RIG-I或MDA5敲低的原代细胞,结果发现,与未敲低的细胞相比,rMHVnsp14-Y414A在RIG-I或MDA5敲低的原代细胞中病毒滴度显著增加,而rMHV的病毒滴度没有变化。同时,研究人员发现,在感染野生型巨噬细胞时,rMHVnsp14-Y414A诱导的IFN-β显著高于rMHV;而在感染Mda5-/-的巨噬细胞时,rMHVnsp14-Y414A和rMHV均不能诱导IFN-β的表达。这些结果表明,MDA5和RIG-I均参与了N7-非甲基化RNA的识别,其中MDA5可能是MHV感染中更重要的识别受体,它们限制了rMHVnsp14-Y414A在原代细胞中的复制(图2)。

图2. rMHV nsp14-Y414A感染的原代细胞中IFN-β的表达依赖于RLR的激活
研究人员进一步利用C57BL/6小鼠检测了rMHV和rMHVnsp14-Y414A的毒力差异,证实rMHVnsp14-Y414A在感染小鼠时致病能力显著下降,呈现明显的减毒表型。同时,在干扰素受体缺失的小鼠体内进行的rMHV和rMHVnsp14-Y414A的感染实验表明,rMHVnsp14-Y414A的毒力部分回复。这些结果表明rMHVnsp14-Y414A毒力的减弱和增强与IFN信号传导密切相关。 此外,Stanley Perlman团队拯救得到了N7-甲基转移酶关键活性位点突变的减毒新冠病毒rSARS-CoV-2nsp14-Y420A,该减毒新冠病毒感染小鼠后,所有小鼠均能够存活,表明rSARS-CoV-2nsp14-Y420A的毒力和致病性显著下降。同时,单次接种rSARS-CoV-2nsp14-Y420A即可保护小鼠免受新冠病毒的再次感染致死,表明rSARS-CoV-2nsp14-Y420A有可能成为一种新的新冠候选疫苗(图3)。
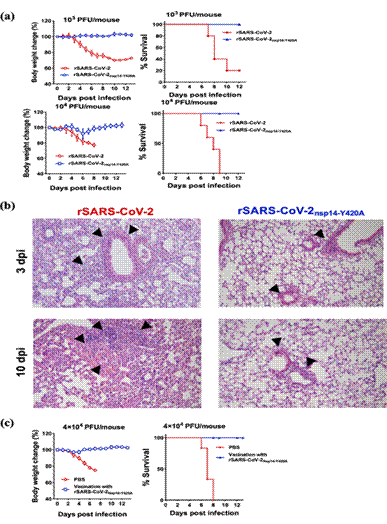
图3. rSARS-CoV-2nsp14-Y420A呈现减毒表型并能够保护小鼠免受致死性SARS-CoV-2攻击
该研究不仅证实了由冠状病毒nsp14介导的RNA N7-甲基化有助于病毒逃避MDA5介导的I型干扰素免疫反应,,还为以冠状病毒N7-甲基转移酶为靶点正向开发冠状病毒减毒活疫苗奠定了理论基础,相关减毒冠状病毒疫苗的概念验证性(proof of concept)研究工作已于前期发表在Emerging Microbes & Infections(Zhang, Z. et al. 2021, Emerging microbes & infections 10, 1626. 论文链接:https://www.tandfonline.com/doi/full/10.1080/22221751.2021.1964385)。
武汉大学生命科学学院博士毕业生潘阮刚、曹流和伯尔尼大学Eveline Kindler博士为该论文共同第一作者;郭德银教授、陈宇教授、Volker Thiel教授和Stanley Perlman教授为该论文共同通讯作者。该研究工作得到了武汉大学新冠科技攻关专项基金、北京泰康溢彩公益基金会、科技部国家重点研发计划、国家自然科学基金新冠病毒专项等项目的资助。
论文链接:https://journals.asm.org/doi/10.1128/mbio.03662-21